|
阅读:5516回复:0
遗传基因诊断检测技术的成本效益分析二代测序技术的发展推动了全基因组测序类基因检测的临床应用,提高了罕见病的诊断率和个体化靶向治疗的发展。在有效的医疗预算前提下,新的基因检测技术和传统的诊断技术互相竞争。这种情况下,基于医疗成本花费的医疗决策模型将成为帮助评估新引入的保健干预措施的成本与收益的有效方法。本文译自Katherine Payne等人在年初发表在 Nature Review Genetics 杂志上的一篇论述,旨在为医疗决策者在面对”如何在日益增多的基因检测技术面前选择最为经济有效的检测手段”这个问题的时候,梳理了一些需要他们考虑的在方法、技术、实践和组织结构方面的层层挑战。 一般来说,基因检测的重点是鉴别导致观察表型(临床表现)的致病单基因变异(医学解释)。这种类型的基因检测形式通常是需要通过提供给遗传病患者诊断、风险评估、咨询、保障和技术支持等的基因检测机构来施行。值得注意的是,目前存在的基因检测机构和模式多种多样,而且不同国家之间又有很大不同。二代测序技术的发展,衍生出了多种基因检测技术,多是基于基因panel,全外显子组测序(WES)和全基因组测序。基因检测技术在一些发达国家,如美国、加拿大、法国、英国等发展迅速,并开始有替代传统检测技术的趋势。 与其它医疗预算的潜在应用相比,选用新的医疗技术所需要的花费及产生的后果(益处和坏处),将有助于医疗决策者进行资源的合理分配(表1)。经济评价方法,如成本有效性(cost-effectiveness analysis,CEA)和成本效益分析(cost-benefit analysis,CBA),可帮助解决这一问题。在一些国家,如澳大利亚、英国,国家决策机构使用成本有效性CEA作为临床指南或赔偿核算的依据。然而,与大多数保健干预措施不同,遗传基因检测技术领域的医疗资源如何分配还没有一个很好的规范。基因检测技术领域的医疗决策者在现有的医疗保健系统的不同层面上进行运作,他们的角色和责任在国家内部和国家之间是不同的。 本篇文章回顾了CEA在提示基因检测是否适用于诊断遗传性罕见疾病或靶向治疗方面时的重要角色,并对国家决策机构实施的评估框架进行了强调。此篇文章回顾了在遗传学基因检测服务中CEA需要考虑的关键因素,特别描述了基于决策分析模型的CEA的潜力,以及它的方法论、技术、实际操作和组织方面面临的层层挑战。 图片:01.jpg
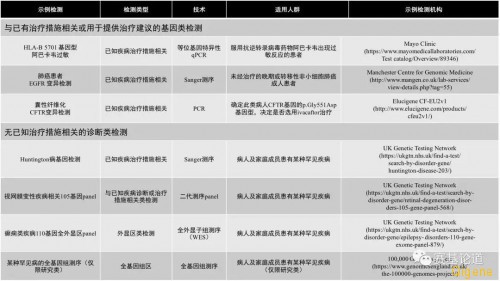
[p][p][p] 表一:基因检测类型示例
[/p][/p][/p][p][p][p][p] 测序费用[/p][/p][/p][/p][p][p][p] 基因检测技术在临床应用的增加通常归功于测序成本的下降,这是由于从Sanger测序转向下一代测序技术所促成的。据美国国家人类基因组研究所(National Human Genome Research Institute, NHGRI)数据显示,截止2007年,全基因组测序费用在1000万美元左右;到了2015年时,该费用已降到了1500美元以下。而在不久的将来,该费用更有望降低到1000美元以下。 但是,类似于这种的成本预测,多聚焦于采购和运行该平台时所需的花费,并没有考虑到下游数据分析和解读的成本。因此,目前人的全基因组测序成本的预估对于决策者来说,其作用还是相对有限的,决策者们需要的是一个对于基因检测行业更加全面的了解,从而更好得使其服务于医疗实践。 类似于Genohub (https://genohub.com/) 类网站,汇总了全球范围的提供二代测序的检测实验室的服务价格,包括全基因组测序($1105~$16420,2017年10月份信息),全外显子组测序($535~$7637),以及基因panel($400–$5,800)。测序类服务所涉及的花费项包括DNA提取、测序覆盖度和深度、测序数据量、测序平台、实验室通用类花销(如管理费用)、技能相关类费用(如,不同水平的实验员的工资)、数据分析解读所需的相关资源,以及提供足够数量检测的能力。
[/p][/p][/p][p][p][p][p] 基因检测的预算影响分析[/p][/p][/p][/p][p][p][p] 将基因检测技术引入健康领域的预算影响分析,以评估大范围应用基因检测技术所涉及的健康领域的资源及潜在对治疗措施的影响,其定量分析要比测序成本分析难的多。迄今为止,还没有公开发表的数据对此进行记载。预算影响分析是预期的当前和未来符合条件的人口规模的函数,而符合条件的人口规模则是根据预期的流行病率或发病率来衡量的。 然而,通过基因检测手段提高疾病诊断率的患者群体人数预计是不定的,而且基因检测还可能会提示补充医学发现信息以致增加额外的医疗花费。而且还要区分基因检测所使用的不同测序技术(如基因panel或是全外显子测序),该技术辅助疾病诊断的稳定性和价值(即它是否有能力提供可信的结果),以及用于向相关病人提供诊断服务的机制(服务交付模式)。即使在一个相对简单的水平,基因检测服务的实际费用也没有得到有效的记录。例如,在英国,提供基因药物的费用是被嵌入专家委托服务内的。但是,对于某一些特定的基因检测类服务,相关性的证据已经开始显现:在英国,将全外显子组测序服务引入到罕见遗传病类患者诊断之前的预算影响分析,与传统诊断措施相比,大概每名患者的花费会增加939英镑(增加约52.5%)。 即使人口规模确定,基因检测的预算影响分析面临的一个根本挑战就是一些国家缺乏透明的国家关税和使用收费,例如每个基因的统一费率,而不是提供检测的费用。
[/p][/p][/p][p][p][p][p] 机会成本[/p][/p][/p][/p][p][p][p] 为某一特定人群分配一项干预措施的资源意味着同样的资源不能再用于照顾其他(已知的或未知的)患者人群。现存的应用于罕见遗传病类基因检测技术的机会成本评估框架与其他的医疗措施不同。针对未经治疗的非小细胞肺癌(NSCLC)成年患者的肿瘤,或如厄洛替尼这类用于治疗局部晚期或转移性非小细胞肺癌当中的药物而进行的EGFR基因突变诊断测试,是通过诊断评估程序和技术评估程序来进行评估的。这两项评估程序均为NICE采用的国家决策框架(图1)的一部分。英国国家健康与照顾卓越研究院(NICE)提倡将选择合适的检测措施和相应的花费都考虑在内,用来计算新的医疗措施在费用和预期后果方面的影响。这种情况下,使用经济学评估,必须考虑两个关键因素:一:这些结果应该可以在人口群体层面上为资源分配决策者提供信息,而不只是在个人层面上协助临床医生或者病人做医疗决定。二:这些结果应作为国家层面上循证实践阶段的信息来源,而不该被视为区域决策者在其管辖权内进行评估的替代品。 图片:02.jpg 图1:决策者示例。 该图显示了提供医疗保健系统的不同级别工作的决策者类型的一些说明。 该图仅显示了几个具有代表性的例子,并不是对卫生保健系统内所有决策者的综合描述。 [/p][/p][/p][p][p][p]多种不同类型的经济评估同时存在,但是在实践应用中,主要存在两种类型的经济评估来量化新干预措施产生的成本和后果:CEA(有时与成本效用分析(CUA)这一术语相互交换)和CBA。如果用经济评估来做出关于决策者“应该做什么”的“应该”陈述,它必须有一些基本的价值判断或规范(“应该是什么”)的原则。CEA和CBA的规范基础分别是超福利主义和福利主义。迄今为止,超福利主义的实际应用,像在NICE评估计划的背景下,支持决策者使用质量调整寿命年(QALYs)来最大程度量化健康。因此,在全球范围内,CEA已经成为指导资源分配和报销决策过程中最为频繁使用的经济评估类型。
[/p][/p][/p][p][p][p][p] 基于试验与基于模型的CEA[/p][/p][/p][/p][p][p][p] 基于试验的CEA与基于模型的CEA存在两种产生数据以进行CEA的方法:基于试验的数据,用于决策的数据通常几乎完全通过单一随机对照试验(RCT)来收集,而基于模型的CEA是从多个不同的来源收集数据,并在经济模型内进行综合。 基于试验的CEA,仅与试验方案有关,在推广到其他司法管辖区或患者群体时具有挑战性。 使用基于模型的CEA允许将所有干预措施和相关比较(例如当前临床实践)包括在内进行分析,结果可以外推以评估干预措施对患者队列的影响,还可以量化不确定性的影响。
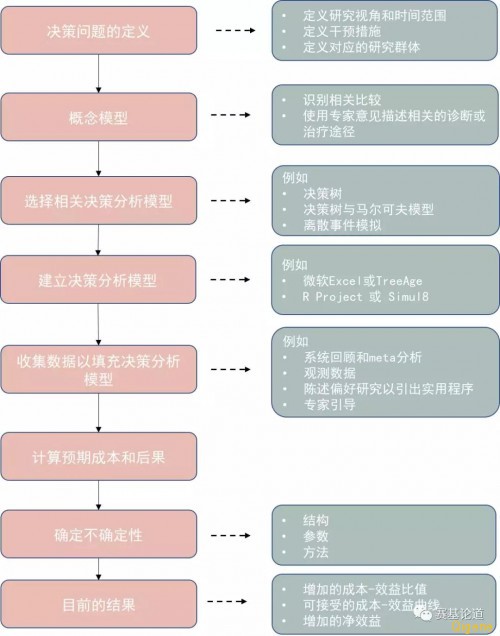
[/p][/p][/p][p][p][p][p] 基于模型的基因检测CEA[/p][/p][/p][/p][p][p][p] 基于模型的基因检测CEA的关键步骤大体上反映了基因诊断试验的那些步骤(图2)。 几个因素必须明确:研究视角、时间范围、对应的研究群体、评估干预及其相关比较。 研究的视角应由最终的用户所定。如果决策者是医院内部职工,那么相应的视角应该是医院的预算。反之,如果国家级别的决策者,则需要一个基于整个医疗体系的研究来分配国家级的医疗预算。研究视角往往受限于医疗系统,因为CEA通常用于国家关于医疗保健预算的成本-效益。 研究的时间范围应该足以使所有相关的成本和后果纳入其中,一般来说,需要使用所定义的病人队列的寿命期限。例如对于癌症靶向治疗的药物效果的研究时间范围,应充分考虑到终生服药的花费和效果。 图片:03.jpg
[/p][/p][/p][p][p][p] 图2:决策分析模型CEA设计与实施中的关键要素[/p][/p][/p][p][p][p]
重要的是,决策问题的定义还包括明确了解相关的患者人群,从而更好得改善干预效果。然而,定义基因检测行业对应的患者人群又是困难重重。例如,考虑到全基因组测序服务的附加值,其对应的患者群体除患者本人之外,其相关家庭成员也应考虑在内。这种情况下,决策问题的定义需要充分考虑附加值,从而明晰基因检测对家庭的额外影响(有时称为溢出效应)。溢出效应又引入了另一个问题,即如何在概念上定义一个生命周期,因为它不再是病人或病人适当的生命周期中容易出现的问题,因为干预的潜在价值可能跨越几代人。 定义决策问题需要明确说明干预和相关的比较。不同的检测也可以被认为是相关的比较。例如,非小细胞肺癌中,针对EGFR基因变异的检测结果不同,服用的靶向治疗药物也不同。现今,针对没有对应治疗方案的以诊断为目的的基因检测技术层出不穷(可参考:https://ukgtn.nhs.uk/find-a-test/)。这种情况,尤其当检测技术涉及到全基因时,就有可能检测到补充医学发现,这种情况下就应考虑如何(是否)将这些信息告知给送检的医生和患者,以及让患者和医生获取对检测技术及分析方法的充分知情。
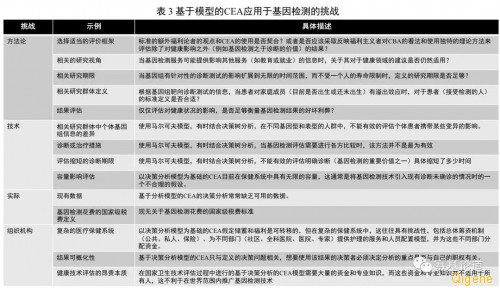
[/p][/p][/p][p][p][p][p] CEA应用于基因检测行业的挑战[/p][/p][/p][/p][p][p][p] 基于模型的CEA应用于基因检测主要面对以下几方面的挑战:1. 是否有已知对应的治疗措施,或者预防的干预手段,如癌症的靶向治疗或者是遗传性癌症等。2. 目前是否没有治疗方案,如某些遗传性罕见病,如共济失调等。 目前关于伴随诊断测试的经济学评估更注重于治疗和预防措施的价值而不是诊断检测结果的价值。目前已经制定了一些关于具体评估诊断试验的附加价值的评估方案,然而,目前CEA中也仍然更注重治疗和预防措施的价值。BOX1展示了基于模型的CEA用于评估有对应治疗方案的医学检测的附加价值。对于没有治疗措施疾病的基因检测,基于模型的CEA还没有给出明确的建议信息。 图片:04.jpg 即使关于罕见疾病进行基因检测的经济学评估文章已有发表,但是基于模型的CEA还没有应用于该领域的医学实践。基于模型的CEA应用于基因检测,尤其是没有可选的治疗措施时,主要存在以下四个方面的挑战(表3): 图片:05.jpg
[p][p][p][p] 结论[/p][/p][/p][/p][p][p][p] 在新的测序技术和国家研究议程的推动下,发达国家中可选用的基因检测技术将会不断增加。考虑到现有服务提供模式和主流医学以外的基因组学潜在的新需求,现存的基因检测的评估框架是不够的。 鉴于医疗保健预算的有限性,决策者需要了解引入新的基因检测的机会成本。基于模型的CEA是HTA程序中嵌入的一个有效工具,用以提供新干预措施的增量成本和后果的明确信息。为了给有关卫生保健资源的有效分配的决策提供信息,基于模型的CEA必须得到强有力的支持和全面的研究,理想情况包含基因检测的三个组成部分:(1)技术;(2)诊断部分;(3)提供诊断类检测甚至是治疗类检测的服务提供模式。遗传学领域具有新兴的经济证据基础。国家研究机构已经适当地开始资助新的基因检测技术的发展,用来取代现有的一些基因检测技术。当前应对以决策分析模型的CEA用于基因检测的研究给予资金支持,同时认识到现有的来自于方法学,技术,实践和机构层面上的挑战,从而最大限度地提高患者群体的潜在收益。[/p][/p][/p][/p][/p][/p][/p][/p][/p] |
|